Temas etmek:Erol Çu (Bay.)
Tel: artı 86-551-65523315
Mobil/WhatsApp: artı 86 17705606359
Soru:196299583
Skype:lucytoday@hotmail.com
E-posta:sales@homesunshinepharma.com
Eklemek:1002, Huanmao Bina, No.105, Mengcheng Yol, Hefei Şehir, 230061, Çin
AbbVie geçtiğimiz günlerde atogepantı migren için değerlendiren Faz III ADVANCE denemesinin birincil son noktasına ulaştığını duyurdu. Veriler, 12 haftalık tedavi süresi boyunca, plasebo ile karşılaştırıldığında, tüm atogepant dozlarının (10 mg, 30 mg, 60 mg) ortalama aylık migren günlerini başlangıç seviyesinden önemli ölçüde azalttığını gösterdi. Ek olarak, iki yüksek doz (30 mg, 60 mg), altı ikincil son noktanın tümünde istatistiksel olarak anlamlı iyileşme gösterdi. AbbVie, bu sonuçların yanı sıra önceki pozitif Faz 2/3 test sonuçlarına dayanarak, Amerika Birleşik Devletleri ve diğer ülkelerde atogepant düzenleyici uygulama belgelerini sunmayı planlamaktadır. Tam veri sonuçları, yaklaşan tıbbi konferansta duyurulacak ve / veya hakemli bir dergide yayınlanacaktır.
Atogepant, özellikle migrenin önleyici tedavisi için geliştirilmiş bir oral kalsitonin geni ile ilişkili peptid (CGRP) reseptör antagonistidir (gepant). CGRP ve reseptörleri, migren patofizyolojisi ile ilgili sinir sistemi alanlarında ifade edilir. Çalışmalar, migren atakları sırasında CGRP düzeylerinin arttığını ve seçici CGRP reseptör antagonistlerinin migren üzerinde klinik etkileri olduğunu göstermiştir.
AbbVie migren alanında BOTOX (Botox®, botulinum toksin A, onabotulinumtoxinA) ve Ubrelvy (ubrogepant) satmaktadır. Bunlar arasında BOTOX, ABD FDA tarafından onaylanan yetişkin kronik migren için ilk koruyucu ilaçtır ve Ubrelvy, yetişkin migren (auralı veya aurasız) için FDA tarafından onaylanan ilk oral CGRP reseptör antagonistidir (gepant). Akut tedavi.
AbbVie Araştırma ve Geliştirme'nin kıdemli başkan yardımcısı ve baş bilim sorumlusu Thomas J. Hudson şunları söyledi: “Migren atakları zayıflatıcı olabilir, ancak migren tedavi edilebilir bir hastalıktır. Bu denemelerin sonuçlarına dayanarak amacımız, hastalara ve sağlık hizmeti sağlayıcılarına CGRP reseptörlerini bloke ederek ve migrenleri önleyerek çalışan basit, günde bir kez oral ilaç sağlayan güvenli ve etkili bir önleyici tedavi sağlamaktır."
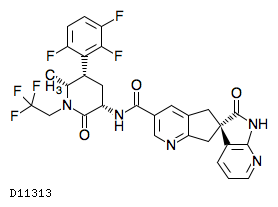
Atogepant kimyasal yapısı (resim kaynağı: genome.jp)
Temel Faz III ADVANCE denemesi hakkında:
Bu, migreni önlemede oral atogepantın etkinliğini, güvenliğini ve tolere edilebilirliğini değerlendirmek için çok merkezli, randomize, çift kör, plasebo kontrollü, paralel grup Faz III çalışmadır. Toplam 910 hasta rastgele 4 tedavi grubuna, 3 doz (10 mg, 30 mg, 60 mg) atogepant ve plasebo olmak üzere günde bir kez oral olarak ayrıldı. Etkililik analizi, 873 hastadan oluşan modifiye edilmiş tedavi amaçlı (mITT) popülasyona dayanıyordu.
Birincil son nokta, 12 haftalık tedavi süresi boyunca taban çizgisine göre aylık ortalama migren günü sayısındaki değişiklikti. Veriler, tüm atogepant doz gruplarının birincil son noktaya ulaştığını ve aylık ortalama migren günü sayısının plaseboya kıyasla istatistiksel olarak önemli ölçüde azaldığını gösterdi. 10 mg / 30 mg / 60 mg atogepant grubu 3,69 / 3. 86 / 4,2 gün azaldı ve plasebo grubu 2,48 gün azaldı (tüm doz gruplarında plasebo grubuna kıyasla, p≤0,0001).
Anahtar bir ikincil son nokta, 12 haftalık tedavi süresi boyunca her ay migren günlerinin sayısında en az% 50 azalma olan hastaların oranını ölçtü. Veriler, 10 mg / 30 mg / 60 mg atogepant grubunun% 55.6 /% 58.7 /% 60.8'inin en az% 50 azaldığını ve plasebo grubundaki hastaların oranının% 29.0 olduğunu gösterdi (tüm dozlarda plasebo grubuna kıyasla grupları, p≤ 0.0001).
12 haftalık tedavi süresi boyunca ölçülen diğer ikincil son noktalar şunları içerir: aylık ortalama baş ağrısı günleri, aylık ortalama akut ilaç kullanım günleri, migren günlük aktivite bozukluğunda (AIM-D) aylık ortalama günlük aktivite performansı ve fiziksel yaralanma alanı Puan Başlangıca göre değişim ve Migrene Özgü Yaşam Kalitesi Anketi (MSQ) rolü fonksiyonel kısıtlama alanı skorunda 12. haftada başlangıca göre değişiklik. Test, 30 mg ve 60 mg doz gruplarının tüm ikincil son noktalar, 10 mg doz grubu ise 6 ikincil sonlanım noktasından 4'ünde istatistiksel olarak önemli gelişmeler göstermiştir.
Güvenlik açısından, atogepant'ı değerlendiren önceki çalışmalarda gözlemlenen güvenliliğe kıyasla hiçbir yeni güvenlik riski gözlenmedi. 10 mg doz grubundaki 0.9 hastada ve plasebo grubunda% 0.9'luk ciddi advers olaylar meydana geldi. 30 mg doz grubunda ve 60 mg doz grubunda hiçbir ciddi yan etki meydana gelmemiştir. En az bir atogepant tedavi grubunda, plasebodan>% 5 ve daha yüksek sıklıkta en yaygın yan etkiler kabızlık (tüm doz gruplarında% 6,9-7,7, plasebo gruplarında% 0,5), bulantı (tüm doz gruplarında 4,4) olmuştur. Plasebo grubunda% -6.1,% 1.8) ve üst solunum yolu enfeksiyonları (tüm doz gruplarında% 3.9-5.7 ve plasebo grubunda% 4.5). Kabızlık, bulantı ve üst emme yolu enfeksiyonu vakalarının çoğu hafif veya orta şiddettedir ve ilacın kesilmesine yol açmamıştır. Bu denemede hiçbir karaciğer güvenliği sorunu bulunmadı.
2/3 CGP-MD-01 çalışması hakkında:
Bu çalışmada oral atogepantın etkinliği, güvenliği ve tolere edilebilirliği değerlendirildi. Veriler, atogepantın tüm tedavi gruplarının birincil son noktaya ulaştığını gösterdi. 12 haftalık tedavi periyodu sırasında, plasebo ile karşılaştırıldığında, aylık ortalama migren günü sayısı başlangıca kıyasla önemli ölçüde azaldı (plaseboya karşı 10 mg QD, p=0.0236; 30 mg QD'ye karşı plasebo P=0.0390; 60 mg QD'ye karşı plasebo, p=0.0390; 30 mg BID, plasebo, p=0.0034; 60 mg BID, plasebo, p=0.0031). Araştırma sonuçları Haziran 2018'de yayınlandı.